Sensore di pressione capacitivo indossabile per la raccolta del segnale fisiologico umano
Sensore di pressione capacitivo indossabile per la raccolta del segnale fisiologico umano
Negli ultimi anni, i sensori di pressione ad alta sensibilità con flessibilità, biocompatibilità ed elasticità hanno attirato un'attenzione diffusa nel campo dei dispositivi elettronici indossabili e delle smart skin. Tuttavia, è una sfida considerevole ottenere sia un'elevata sensibilità che un basso costo del sensore e ottenere la migliore stabilità meccanica e un limite di rilevamento ultra basso per l'uso in delicate apparecchiature di monitoraggio del segnale fisiologico. In risposta ai problemi di cui sopra, questo articolo riporta un semplice metodo di preparazione di un sensore di pressione capacitivo (CPS) ad alta sensibilità e alta affidabilità per la misurazione della pressione ultrabassa. TrFE) impalcatura composita di nanofibre (CNS) inserita tra elettrodi biocompatibili di poli (3,4-etilendiossitiofene) polistirene solfonico (PEDOT: PSS)/polidimetilsilossano (PDMS) tra gli elettrodi come uno strato dielettrico. Il sensore preparato ha un'elevata sensibilità di 0,51 kPa-1 e un limite di rilevamento minimo di 1,5 Pa. Inoltre, può anche ottenere un rilevamento lineare in un ampio intervallo di pressione (0-400 kPa) e raggiungere un'elevata affidabilità durante 10.000 cicli anche ad altissima pressione (maggiore di 167 kPa). Rispetto allo scaffold originale in nanofibra PVDF-TrFE, la sensibilità del sensore basato su nanofibra può essere migliorata caricando con MXene, aumentando così la costante dielettrica a 40 e riducendo il modulo di compressione al 58%. Questo sensore può determinare la salute dei pazienti monitorando i segnali fisiologici (frequenza del polso, respirazione, movimento muscolare e contrazioni oculari) ed è un buon candidato per la prossima generazione di dispositivi di interfaccia uomo-macchina. può anche ottenere un rilevamento lineare in un ampio intervallo di pressione (0-400 kPa) e raggiungere un'elevata affidabilità durante 10.000 cicli anche a pressioni ultra elevate (maggiori di 167 kPa). Rispetto allo scaffold originale in nanofibra PVDF-TrFE, la sensibilità del sensore basato su nanofibra può essere migliorata caricando con MXene, aumentando così la costante dielettrica a 40 e riducendo il modulo di compressione al 58%. Questo sensore può determinare la salute dei pazienti monitorando i segnali fisiologici (frequenza del polso, respirazione, movimento muscolare e contrazioni oculari) ed è un buon candidato per la prossima generazione di dispositivi di interfaccia uomo-macchina. può anche ottenere un rilevamento lineare in un ampio intervallo di pressione (0-400 kPa) e raggiungere un'elevata affidabilità durante 10.000 cicli anche a pressioni ultra elevate (maggiori di 167 kPa). Rispetto allo scaffold originale in nanofibra PVDF-TrFE, la sensibilità del sensore basato su nanofibra può essere migliorata caricando con MXene, aumentando così la costante dielettrica a 40 e riducendo il modulo di compressione al 58%. Questo sensore può determinare la salute dei pazienti monitorando i segnali fisiologici (frequenza del polso, respirazione, movimento muscolare e contrazioni oculari) ed è un buon candidato per la prossima generazione di dispositivi di interfaccia uomo-macchina. Rispetto allo scaffold originale in nanofibra PVDF-TrFE, la sensibilità del sensore basato su nanofibra può essere migliorata caricando con MXene, aumentando così la costante dielettrica a 40 e riducendo il modulo di compressione al 58%. Questo sensore può determinare la salute dei pazienti monitorando i segnali fisiologici (frequenza del polso, respirazione, movimento muscolare e contrazioni oculari) ed è un buon candidato per la prossima generazione di dispositivi di interfaccia uomo-macchina. Rispetto allo scaffold originale in nanofibra PVDF-TrFE, la sensibilità del sensore basato su nanofibra può essere migliorata caricando con MXene, aumentando così la costante dielettrica a 40 e riducendo il modulo di compressione al 58%. Questo sensore può determinare la salute dei pazienti monitorando i segnali fisiologici (frequenza del polso, respirazione, movimento muscolare e contrazioni oculari) ed è un buon candidato per la prossima generazione di dispositivi di interfaccia uomo-macchina.
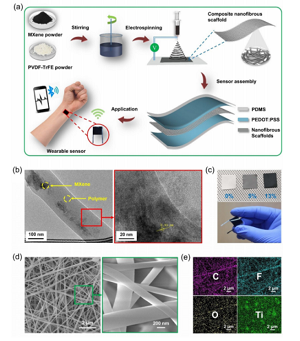
Figura 1. Processo di preparazione e struttura del sensore di pressione basato su CNS. (A) Mostra il diagramma schematico del processo di preparazione del sensore di pressione basato su CNS. (B) Immagine TEM del sistema nervoso centrale, che mostra il nanoflake di MXene a strato singolo e multistrato. L'inserto è un TEM ad alta risoluzione che mostra la spaziatura interstrato di 0,93 nm corrispondente al piano MXene (002). (C) La foto mostra il SNC di diverse concentrazioni di MXene e il sensore prodotto. (D) Immagine FESEM del SNC. L'inserto mostra la morfologia a maggiore ingrandimento. (E) Il diagramma EDS delle nanofibre composite mostra gli elementi C, F, O e Ti.
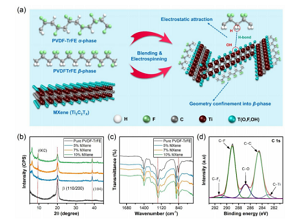
Figura 2. Caratteristiche schematiche e di superficie del SNC. (A) Un diagramma schematico che mostra la sinergia ottenuta dopo aver introdotto MXene nella matrice polimerica. (B,c) Analisi XRD e FTIR del SNC a varie concentrazioni di MXene. (D) Spettro XPS della regione C 1s del SNC contenente il 5% in peso di concentrazione di MXene.
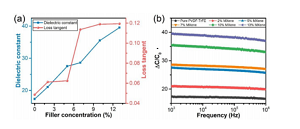
Figura 3. Caratteristiche elettriche di diversi campioni (a) La costante dielettrica e la tangente di perdita del CNS rispetto al contenuto di MXene (in peso%). (B) Dipendenza dalla frequenza della costante dielettrica.
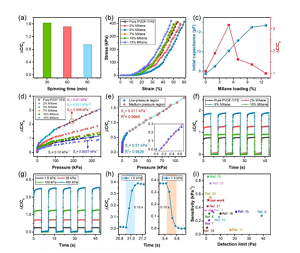
Figura 4. Caratteristiche elettromeccaniche dei sensori di pressione basati su CNS. (A) Confronto delle prestazioni di sensori basati su CNS in base a diversi tempi di elettrofilatura. (B) Le prestazioni di sollecitazione-deformazione di compressione del sensore sotto un carico stabile con una distanza di compressione fino a 0,4 mm. (C) La capacità iniziale (C0) e la variazione relativa (ΔC/C0) del sensore basato su CNS dipendono dal contenuto di MXene (in peso%). (D) La variazione di capacità relativa (ΔC/C0) dei sensori basati su CNS contenenti strati dielettrici con diverse concentrazioni di MXene (in % in peso) a una distanza di compressione costante di 0,4 mm. (E) Un grafico descrittivo di ΔC/C0, che illustra la sensibilità alla pressione ottenuta quando il carico di MXene è del 5% in peso. L'illustrazione mostra la sensibilità del sensore nell'area di bassa pressione. (F) Per diverse concentrazioni di MXene, la risposta della capacità ciclica (carico/scarico) dei sensori basati su CNS a una distanza di compressione costante di 0,3 mm e (g) a diversi valori di pressione di carico/scarico, la concentrazione di MXene è il 5% in peso della risposta della capacità ciclica del SNC sensore basato. (H) Tempo di risposta e rilassamento in un ciclo di carico/scarico con una pressione di 1,5 kPa. (I) Rispetto al rapporto precedente, le prestazioni del sensore in termini di sensibilità riportate ai limiti di rilevamento bassi nell'intervallo di bassa pressione.
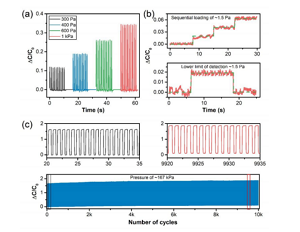
Figura 5. (a) La variazione relativa della risposta di capacità in cicli di carico e scarico a bassa tensione. (B) Illustrare il limite inferiore di rilevamento (LOD) caricando e scaricando in sequenza circa 38 mg di riso a chicco lungo. (C) Test di stabilità ciclica del sensore di pressione basato su CNS dopo 10.000 cicli di carico e scarico ad alta pressione di circa 167 kPa (compressione superiore al 40%). Il riquadro mostra il ciclo selezionato all'inizio e alla fine del test di stabilità.
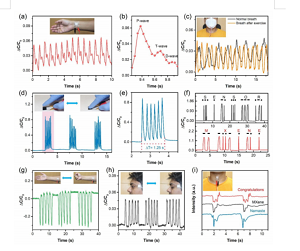
Figura 6. L'applicazione di sensori basati sul SNC nel monitoraggio continuo e in tempo reale dei segnali fisiologici umani. (A) Monitoraggio in tempo reale dell'onda del polso arterioso. Illustrazione: foto del sensore attaccato all'area cutanea del polso. (B) Una vista ingrandita di una singola forma d'onda di impulso, comprese informazioni dettagliate sui suoi picchi caratteristici. (C) Monitorare la respirazione prima e dopo l'esercizio. Illustrazione: una foto di un sensore collegato a una maschera per monitorare la frequenza respiratoria. (D) Il diagramma mostra che il sensore simula il tocco delle dita a una frequenza di tremore statico di 4,8 Hz per rilevare la malattia di Parkinson primaria. Illustrazione: una foto che imita un dito che tocca la superficie del sensore a una frequenza costante. (E) Un'immagine ingrandita che simula le percussioni a una specifica frequenza di tremore di 4,8 Hz. (F) Una pressione breve e lunga sul sensore può generare un segnale di codice Morse internazionale. (G) Monitorare la contrazione e l'espansione muscolare aprendo e chiudendo reversibilmente il pugno. Illustrazione: foto del sensore attaccato ai muscoli addominali del polso. (H) Monitorare il segnale generato dalla vibrazione dei muscoli oculari durante le contrazioni oculari. Illustrazione: una foto del sensore attaccato alla pelle dell'occhio. (I) La capacità del sensore di riconoscere suoni diversi con forme d'onda ripetitive e diverse. Illustrazione: foto del sensore attaccato all'epidermide della gola. (H) Monitorare il segnale generato dalla vibrazione dei muscoli oculari durante le contrazioni oculari. Illustrazione: una foto del sensore attaccato alla pelle dell'occhio. (I) La capacità del sensore di riconoscere suoni diversi con forme d'onda ripetitive e diverse. Illustrazione: foto del sensore attaccato all'epidermide della gola. (H) Monitorare il segnale generato dalla vibrazione dei muscoli oculari durante le contrazioni oculari. Illustrazione: una foto del sensore attaccato alla pelle dell'occhio. (I) La capacità del sensore di riconoscere suoni diversi con forme d'onda ripetitive e diverse. Illustrazione: foto del sensore attaccato all'epidermide della gola.




